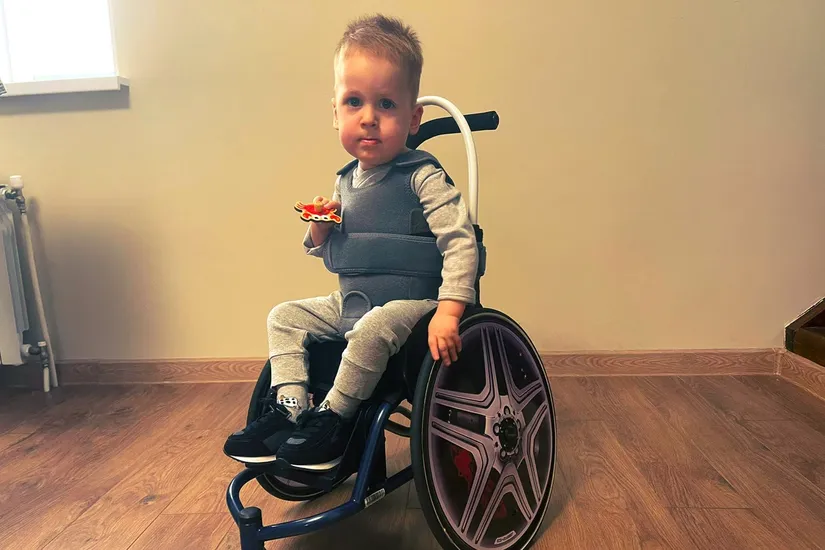
Казалось, что этот укол навсегда остановит СМА, и скоро Миша встанет на ножки и побежит по…
Продолжить чтениеМетка: SMN2

Эксперты предложили новый метод лечения детей со спинальной мышечной атрофией
Эксперты предлагают начинать лечение детей с СМА до появления первых признаков болезни. Эксперты считают, что ранее…
Препарат «Золгенсма» противопоказан в 25-30% случаев СМА
Препарат для лечения спинальной мышечной атрофии «Золгенсма» показан только при условии наличия трёх и менее копий…
Забота о «смайликах»: что будет с лекарствами от СМА?
Фармацевтическому рынку России ничто не угрожает. Об этом на неделе заявили в Минздраве. Несмотря на западные…
В России стартовал набор в клиническое исследование DEVOTE повышенных дозировок нусинерсен при СМА
В середине августа 2021 года в двух российских центрах стартовало клиническое исследование — DEVOTE препарата Нусинерсен…

Самое частое из редких. Как лечат генную мутацию?
Отчего мышцы слабеют? Редкие (орфанные) заболевания — это особая категория, включающая те болезни, которые диагностируются у малого количества пациентов.…

Спинальная мышечная атрофия (СМА): ответы на самые часто задаваемые вопросы
Эту болезнь называют самой частой из редких. Она встречается у одного новорождённого из 6 000-10 000.…
Продолжить чтение
Для спинальной мышечной атрофии подбирают новые лекарства
Менее токсичные более стабильные аналоги нусинерсена могут заменить его в лечении СМА. При спинальной мышечной атрофии…
Продолжить чтение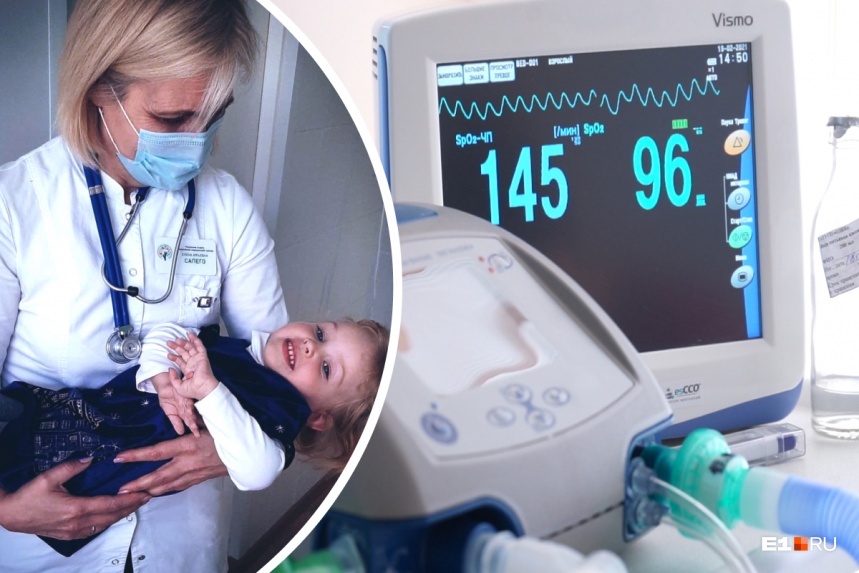
В каждом классе есть один носитель болезни: что такое СМА и как ее распознать
Врач рассказал о вероятности рождения ребенка со СМА О том, каковы риски рождения ребенка со СМА,…
Продолжить чтение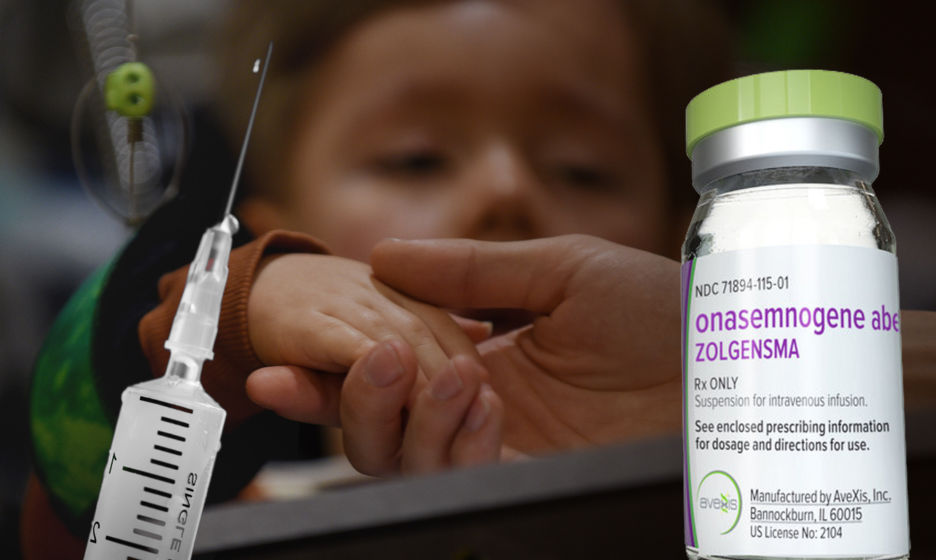
Европейским врачам разрешили генную терапию для больных СМА. Это непомерно дорого, но может спасти жизни
Европейские врачи дали добро на использование препарата «Золгенсма» для тех, кто страдает спинальной мышечной атрофией. Правда,…
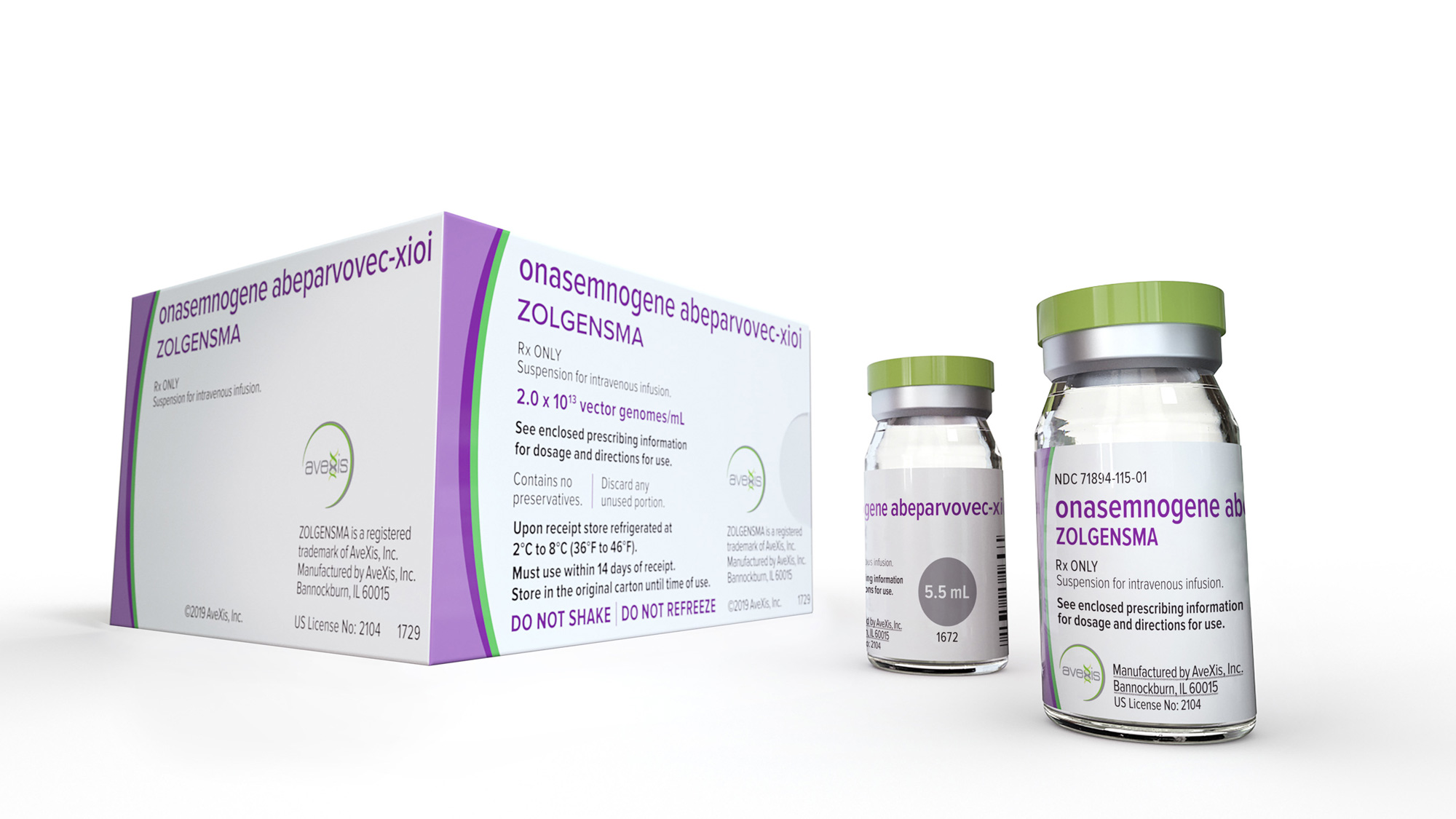
В Европе одобрили препарат «Золгенсма» для лечения СМА. Это самое дорогое лекарство в мире
Европейская комиссия одобрила препарат Zolgensma («Золгенсма») для лечения спинальной мышечной атрофии (СМА), разработчиком которого является компания…

«Янссен» поддержит программу бесплатной диагностики спинальной мышечной атрофии
«Янссен», подразделение фармацевтических товаров ООО «Джонсон & Джонсон», объявляет о запуске программы бесплатной диагностики спинальной мышечной…
Продолжить чтение
«Иногда у ребенка нет и дня». В России больше двух тысяч больных СМА. Им нужна помощь государства
Спинально-мышечная атрофия — заболевание настолько тяжелое, а лечение — дорогостоящее, что в России пометка «детей со…
Продолжить чтение
Юлия Латынина: Про медицину у нас и у них. СМА
… И я хочу начать с истории, которая началась в «Новой газете». В январе «Новая газета»…
Продолжить чтение
Самое дорогое лекарство в мире. Как лечат детей со СМА и почему Россия хуже Румынии
В России 20 (двадцать) детей, больных СМА, в возрасте до 2 лет. Вылечить каждого из них…
Продолжить чтение
Риздиплам – разрабатываемое лечение для Спинальной мышечной атрофии (тип 2,3). Положительные результаты
Положительные результаты исследований препарата Риздиплам для Спинальной мышечной атрофии (СМА) 2 и 3 типов 10 ноября…
Продолжить чтение
Risdiplam демонстрируют постоянную пользу для пациентов со спинальной мышечной атрофией
2 октября были представлены новые данные, демонстрирующие постоянную пользу рисдиплама (RG7916) для лечения всех типов спинальной мышечной…
Продолжить чтение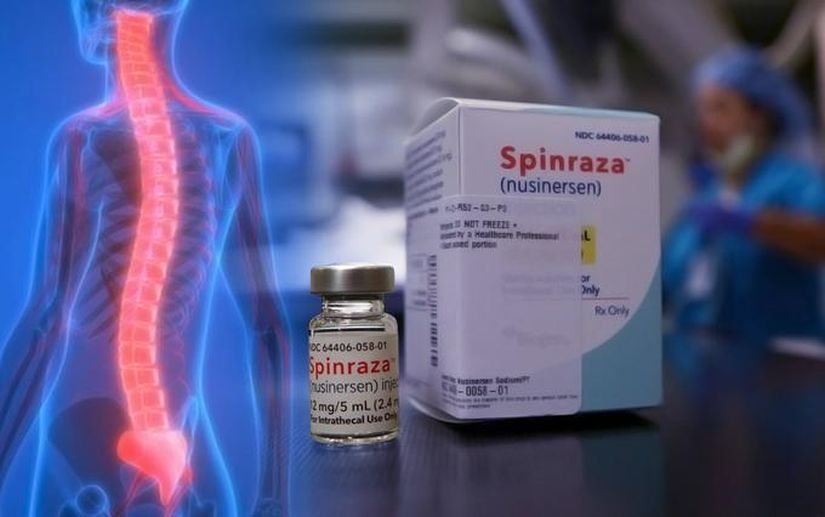
Чем нас лечат: Спинраза. Против СМА и смысла
Работает ли первый в стране препарат от спинальной мышечной атрофии. В чем Спинраза превзошла все ожидания…
Продолжить чтение