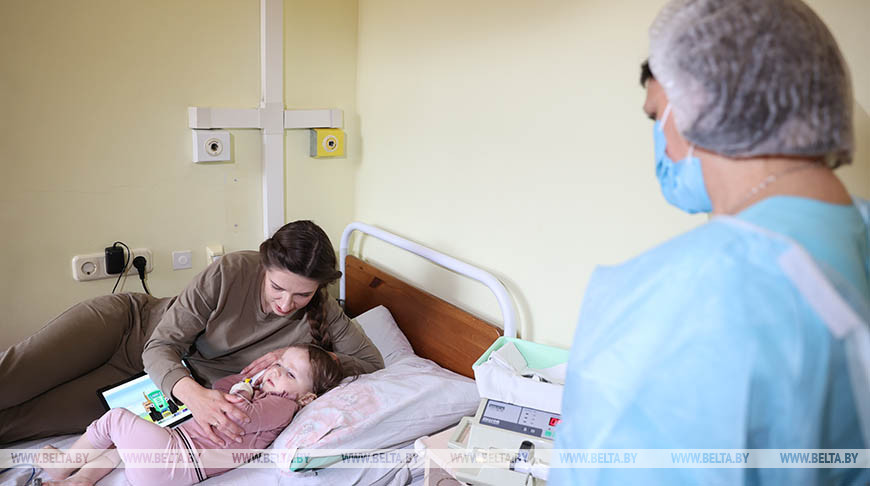
В РНПЦ «Мать и дитя» в Республиканском центре наследственных нервно-мышечных заболеваний специалисты вводят малышке генное лекарственное…
Метка: AVXS-101

«Болезнь остановлена». История Даши, которой первой в Беларуси сделали самый дорогой укол в мире
Даше Шепетовской всего год и четыре месяца, но она уже вошла в историю Беларуси. Год назад родители малышки узнали,…
Продолжить чтение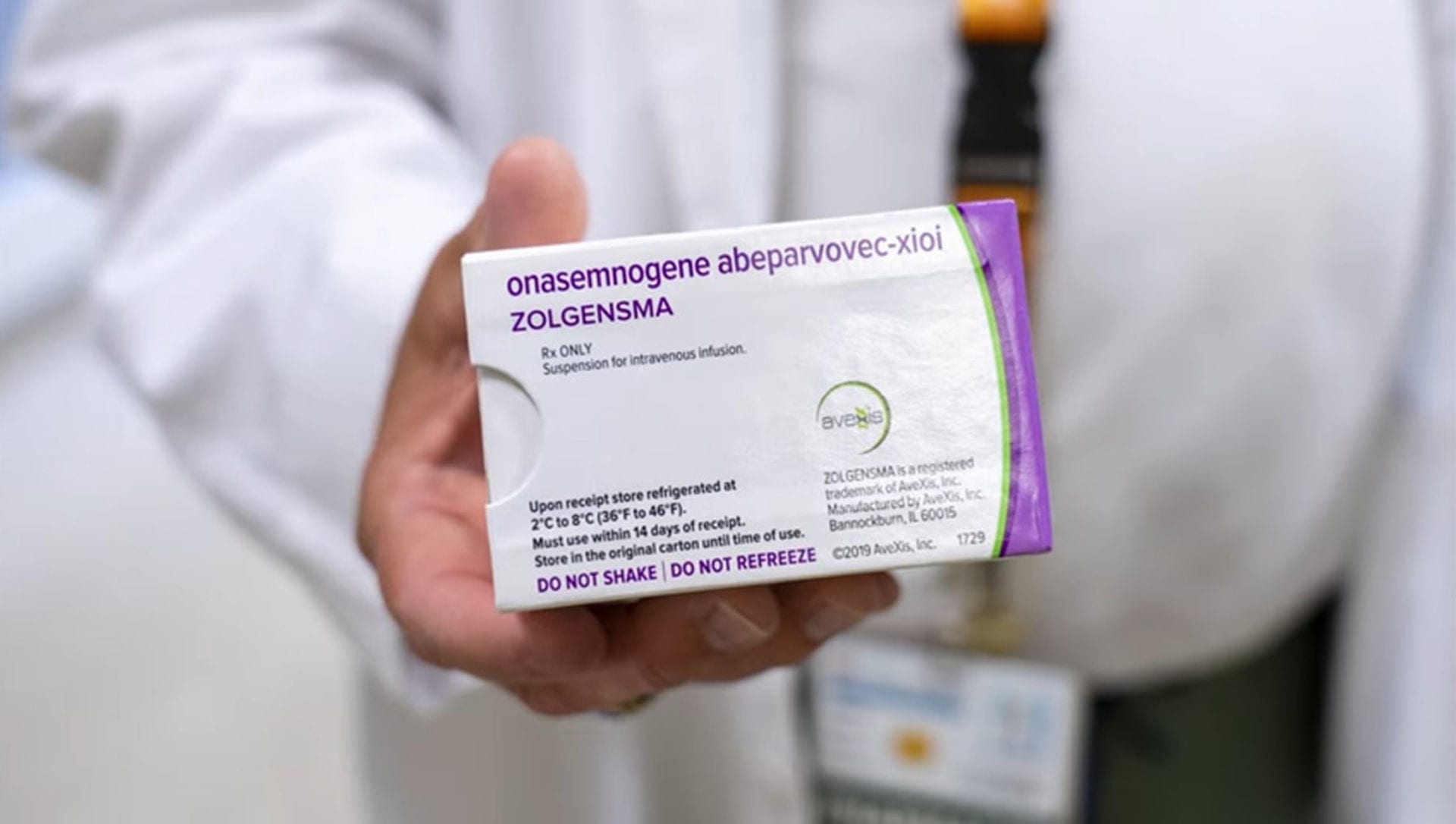
«Первый в истории страны случай». В Беларуси ребенку со СМА ввели самый дорогой в мире генный препарат
В РНПЦ «Мать и дитя» 17 декабря ребенку со спинальной мышечной атрофией впервые в стране ввели самый дорогой в мире генный препарат —…
Денег нет, но детей лечат. Как небогатая Польша смогла поставить борьбу с СМА на поток
Польша — не самая благополучная страна Европы. К тому же в здравоохранении там, по мнению моих…
Продолжить чтение
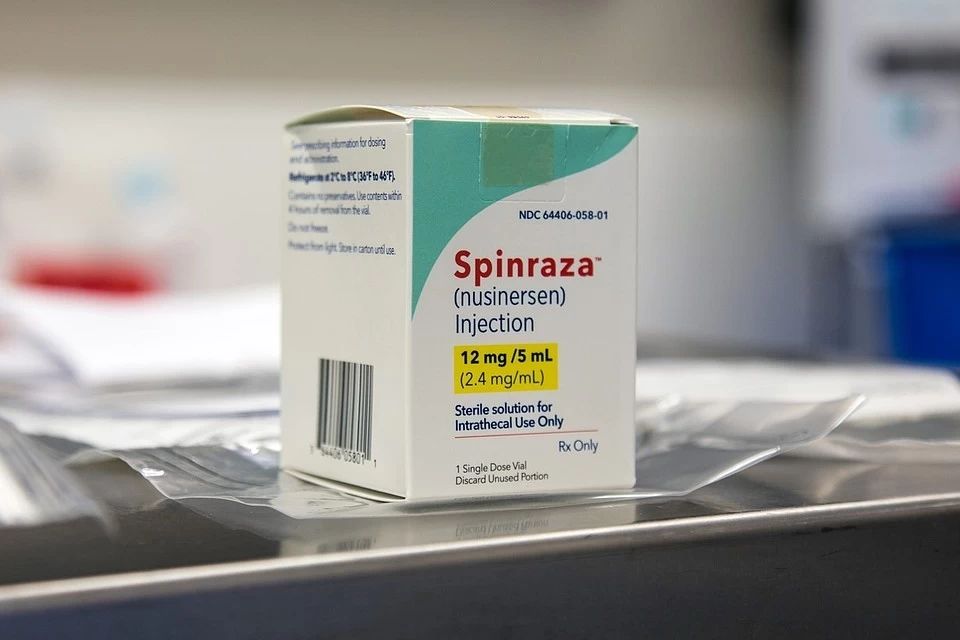
Чем нас лечат: Спинраза. Против СМА и смысла
Работает ли первый в стране препарат от спинальной мышечной атрофии. В чем Спинраза превзошла все ожидания…
Продолжить чтение
ZOLGENSMA (AVXS-101): текущая информация и ответы на вопросы о статусе препарата в настоящее время
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов в США (FDA) объявило, что рассмотрит…
Продолжить чтение
Zolgensma (AVXS-101) в рамках приоритетного анализа FDA в качестве возможной генной терапии для SMA типа 1
Администрация по контролю за продуктами и лекарствами США (FDA) предоставила приоритетный обзор заявке на биологическую лицензию Novartis (BLA) с…
Продолжить чтение
Novartis вложит $8,7 млрд в генную терапию
Швейцарский фармпроизводитель Novartis покупает биотехнологическую компанию AveXis, которая занимается генной терапией спинальной мышечной атрофии. Общая сумма…
Продолжить чтение
«Ни Спинраза, ни генная терапия не являются панацеей»: достижения, надежды и ограничения терапии СМА
«Исследователи начинают накапливать данные по долгосрочному наблюдению», говорит Финкель. Данные о детях СМА типа 2 сейчас…
Продолжить чтение