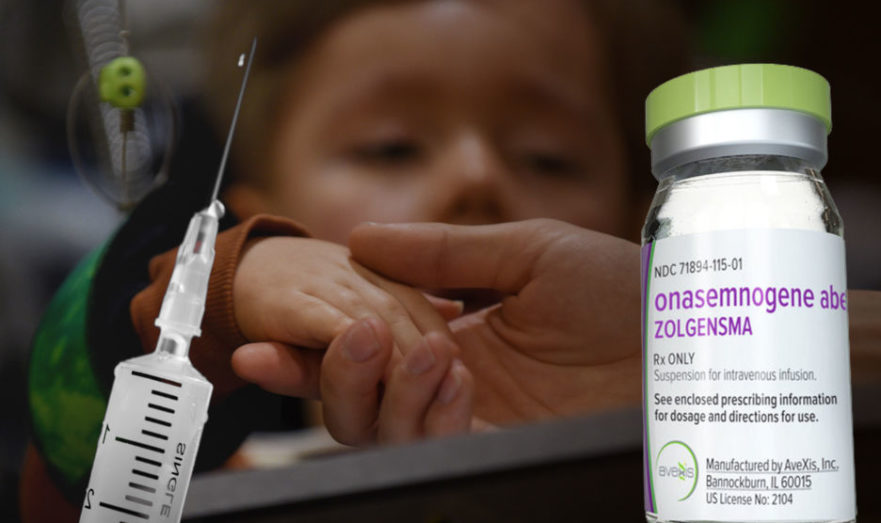
Экспертный совет фонда «Круг добра» предложил закупить для терапии миодистрофии Дюшенна (МДД) не зарегистрированные в России…
Продолжить чтениеМетка: BioMarin

Важнейшие новости фармакологии и медицинских биотехнологий за вторую половину 2016 года
Здание компании Novartis в Базеле, Швейцария. В этом году созданный ею препарат показал успехи в борьбе с рассеянным склерозом. Предлагаем…
Продолжить чтение
Первое лекарство от миопатии Дюшенна может появиться в США в 2016 году
Управление по продуктам и лекарствам США (FDA) отложило рассмотрение заявки американской биофармацевтической компании BioMarin Pharmaceutical Inc,…
Продолжить чтение
Етеплирсен & Дрисаперсен: Два препарата для лечения миодистрофии на горизонте.
В понедельник, 29 июня BioMarin объявила, что FDA приняла заявку на регистрацию нового препарата (NDA) для…

BioMarin завершает представление информации для ускоренного одобрения дрисаперсена для лечения мышечной дистрофии Дюшенна.
Заявление сотрудника научной программы АМД Лауры Хагерти: «Это очень обнадеживающие новости для сообщества МДД, и мы…