Экспертный совет фонда «Круг добра» предложил закупить для терапии миодистрофии Дюшенна (МДД) не зарегистрированные в России препараты: Vyondys 53 (golodirsen), Exondys 51 (eteplirsen) и Viltepso (viltolarsen). Также было выдвинуто предложение по закупке лексредства Oxlumo (lumasiran), предназначенного для терапии оксалоза (первичной гипероксалурии) первого типа.
Препараты Vyondys 53 и Exondys 51 разработаны Sarepta Therapeutics. Оба лексредства помогают организму вырабатывать белок дистрофин, функция которого заключается в стабилизации структуры мышечной ткани. Vyondys 53 корректирует генную мутацию путем пропуска экзона 53 (участок ДНК), Exondys 51 – путем пропуска экзона 51.
В 2016 году Управление по контролю за продуктами и лекарствами США (FDA) одобрило eteplirsen по ускоренной процедуре. Он может использоваться для лечения около 14% случаев МДД. В 2019 году FDA выдало разрешение на использование препарата Vyondys 53. Он рекомендован примерно для 8% пациентов с МДД.
В США стоимость Vyondys 53 или Exondys 51 в дозировке 100 мг составляет $1,6 тысячи (рекомендовано 30 мг/кг). Каждое из лексредств вводится внутривенно один раз в неделю, то есть для пациентов с массой тела 40 кг годовой курс терапии любым из препаратов обойдется в $1,4 млн.
Viltepso разработан NS Pharma, входящей в японскую Nippon Shinyaku. Медикамент, как и Vyondys 53, корректирует генную мутацию, пропуская экзон 53. Он одобрен FDA по ускоренной процедуре в 2020 году, в том же году он получил условное маркетинговое разрешение в Японии. В США оптовая цена за один флакон (250 мг) Viltepso составляет $1,4 тысячи, препарат вводится внутривенно один раз в неделю, рекомендовано 80 мг/кг, таким образом стоимость годового курса Viltepso составляет $733 тысячи для пациентов с весом 30 кг. В Японии цена за один флакон Viltepso составляет 91,1 тысяч иен ($850).
В настоящее время отсутствуют доказательства явной клинической эффективности всех трех препаратов. На данный момент для терапии МДД фондом «Круг добра» к закупке уже утверждено лексредство Трансларна от PTC Therapeutics.
Разработчиком Oxlumo является Alnylam Pharmaceuticals. В ноябре 2020 года Европейское агентство по лекарственным средствам (EMA) выдало компании разрешение на продажу препарата, следом FDA разрешило его к применению. Оба регулятора одобрили препарат для пациентов любого возраста.
Через несколько дней после одобрения Oxlumo американским регулятором в интервью FiercePharma генеральный директор компании –разработчика лексредства Джон Мараганор заявил, что Alnylam Pharmaceuticals оценивает стоимость препарата в среднем в $493 тысячи на пациента в год и ожидает, что окончательная цена годового курса будет составлять около $380 тысяч на пациента.
Оксалоз первого типа и нейрональный цероидный липофусциноз (НЦЛ) второго типа «Круг добра» включил в перечень заболеваний, терапия которых будет финансироваться за его счет, в конце июня. Для терапии НЦЛ экспертный совет организации предложил препарат Brineura от BioMarin.
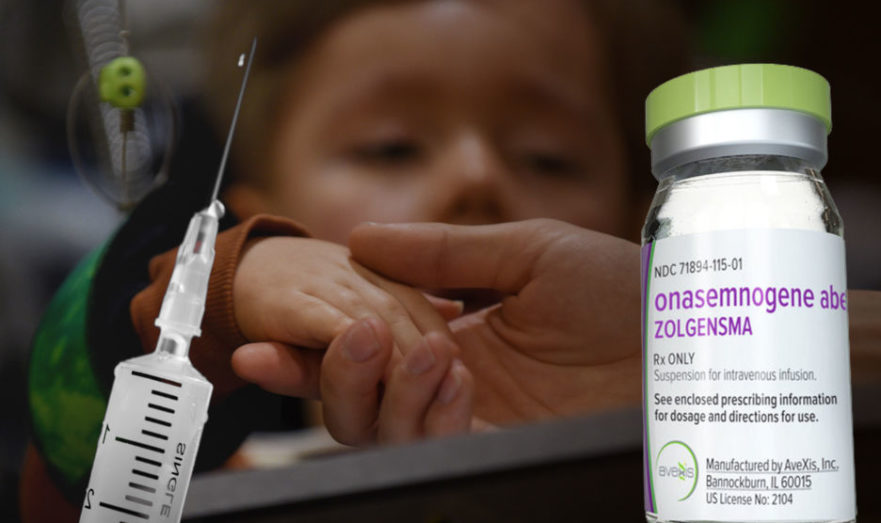
Первым не зарегистрированным в РФ лексредством, сбор заявок на которое начал фонд, стала Золгенсма, предназначенная для терапии спинальной мышечной атрофии.
Глава фонда «Круг добра» Александр Ткаченко 9 июля сообщил, что родители пациентов в скором времени смогут отслеживать подаваемые в фонд заявки на лекарства на специальной информационной платформе и в перспективе – на портале госуслуг.
«Наша информационная система, которая позволяет регионам подавать заявки, а законному представителю получать максимально быстро информацию о статусе рассмотрения заявки, начала работать в режиме тестирования в четырех регионах. В ближайшее время, надеемся, что на следующей неделе, все регионы подключатся к этой системе. В течение месяца-двух эта система будет подключена к порталу госуслуг. И законные представители, пройдя идентификацию, смогут получать информацию о заявке: прошла согласование, прошла рассмотрение, направлено на закупку, поступило в учреждение для лечения по месту проживания ребенка», – пояснил Ткаченко.
Источник https://www.vademec.ru