В Москве начали применять новую терапию для лечения беременных женщин, инфицированных коронавирусом. Специалисты применяют препараты из…
Продолжить чтениеМетка: плацебо

Испытания показали, что Vamorolone безопасным образом улучшает мышечную функцию у детей с МДД
Опубликованы ключевые данные второй фазы испытания (2 b) VISION-DMD. Результаты показали эффективность Vamorolone наряду с главной…
Продолжить чтение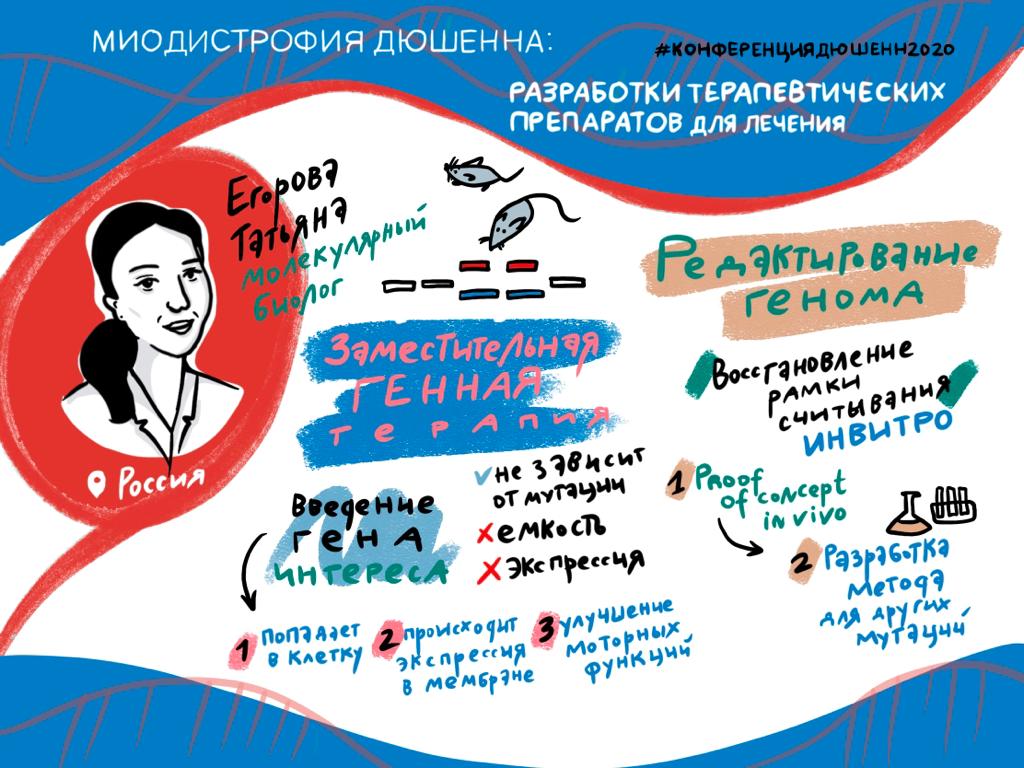
Лечение миодистрофии Дюшенна: настоящее и будущее терапии
Генетики мировых лабораторий активно работают над проблемой лечения миодистрофии Дюшенна (МДД). Эксперты рассказали участникам первой Всероссийской…
Продолжить чтение
Минздрав одобрил вакцину «Спутник V» для применения у людей старше 60 лет
Вакцина Гам-КОВИД-Вак «Спутник V» одобрена Минздравом Беларуси для применения у людей старше 60 лет На сегодняшний…
Продолжить чтение
Итальфармако откладывает испытание фазы 3 гивиностата при МДД из-за COVID-19
Из-за глобальной пандемии COVID-19 Итальфармако приостановила регистрацию мальчиков с мышечной дистрофией Дюшенна (МДД) в фазу 3…
Продолжить чтение
Эффект массажа икры у мальчиков с мышечной дистрофией Дюшенна
Мы исследовали эффекты стандартизированного массажа икры у мальчиков с мышечной дистрофией Дюшенна (МДД), используя проспективный дизайн…

Риздиплам – разрабатываемое лечение для Спинальной мышечной атрофии (тип 2,3). Положительные результаты
Положительные результаты исследований препарата Риздиплам для Спинальной мышечной атрофии (СМА) 2 и 3 типов 10 ноября…
Продолжить чтение
Рисдиплам безопасен и эффективен при лечении СМА 2 и 3 типа
В скором времени в мире может появиться новое высокоэффективное средство для лечения спинальной мышечной атрофии, так…
Продолжить чтение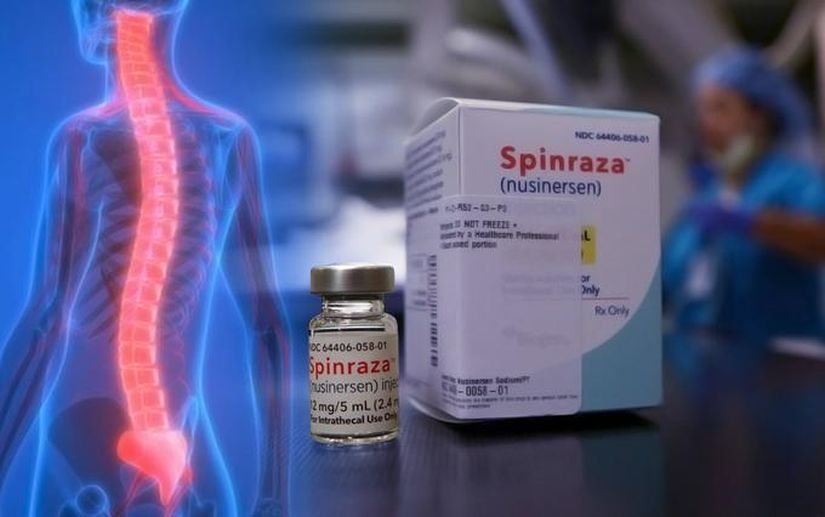
Чем нас лечат: Спинраза. Против СМА и смысла
Работает ли первый в стране препарат от спинальной мышечной атрофии. В чем Спинраза превзошла все ожидания…
Продолжить чтение
SRK-015, экспериментальный препарат для терапии СМА, влияющий на мышечную функцию, показал положительные результаты в первой фазе клинических исследований
Компания Scholar Rock на днях объявила о положительных промежуточных результатах первой фазы испытаний препарата для терапии…
Продолжить чтение
Новые данные о планах по регистрации досье на препарат Рисдиплам для лечения СМА
7 января компания PTC Therapeutics, Inc в рамках презентации на 37-й ежегодной конференции JP Morgan Healthcare…
Продолжить чтение
Подходы к лечению мышечной дистрофии Дюшенна, которые обсуждались на конференции PPMD
Дискуссия о работе над четырьмя различными подходами к лечению мышечной дистрофии Дюшенна (DMD) — восстановлению или…
Продолжить чтение
В США неизлечимо больным разрешили пользоваться экспериментальными лекарствами
В США неизлечимо больным разрешили пользоваться «сырыми» экспериментальными лекарствами. А что можно россиянам в подобной ситуации?…
Продолжить чтение
Обновленный статус исследовательских программ в области СМА компании Roche
В настоящий момент компания Roche ведет клинические разработки 2 молекул для терапии спинальной мышечной атрофии (СМА)…
Продолжить чтение
Компания Summit Therapeutics обьявила данные 2 Фазы 24 недельного клинического исследования препарата Ezutromid
Компания Summit Therapeutics обьявила данные 2 Фазы 24 недельного клинического исследования препарата Ezutromid (регулятор утрофина), где…
Продолжить чтение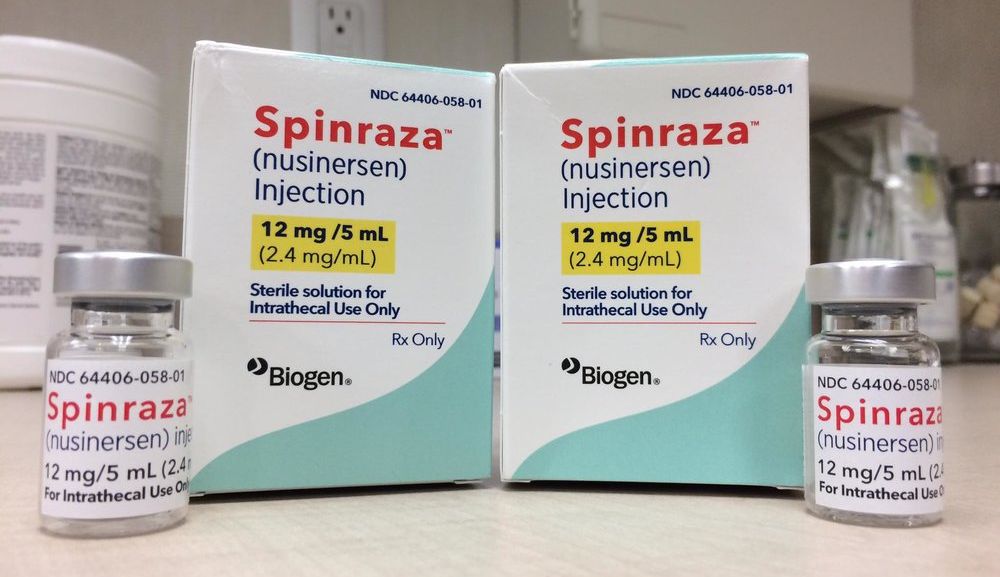
«Ни Спинраза, ни генная терапия не являются панацеей»: достижения, надежды и ограничения терапии СМА
«Исследователи начинают накапливать данные по долгосрочному наблюдению», говорит Финкель. Данные о детях СМА типа 2 сейчас…
Продолжить чтение
Сообщается о значительных улучшениях у пациентов с МДД, которые участвуют в клинических исследованиях клеточной терапии Capricor
Мальчики и юноши на поздних стадиях мышечной дистрофии Дюшенна показывают значительное и устойчивое улучшение сердечной структуры…
Продолжить чтение
Два мальчика против государства: суд не на жизнь, а на смерть
Заболевание обрекает их на смерть в возрасте примерно 20 лет. Лекарство, способное продлить жизнь, уже применяется…
Продолжить чтение