Компания Avidity Biosciences сообщила, что её препарат дель-зота (для пациентов с делециями, корректируемыми пропуском экзона 44)…
Продолжить чтениеМетка: FDA

Заявление компании Sarepta о возобновлении поставок и лечения препаратом Элевидис для амбулаторных пациентов с МДД
FDA рекомендует компании Sarepta возобновить поставки препарата ЭЛЕВИДИС для амбулаторных пациентов с мышечной дистрофией Дюшенна — Компания благодарит…
Продолжить чтение
Поставки препарата для пациентов с миодистрофией Дюшенна временно приостановят
Компания Roche временно приостановит некоторые поставки в ряд стран за пределы США препарата генозаместительной терапии «Элевидис»,…
Продолжить чтение
Sarepta сообщила о второй смерти пациента после генной терапии
Американская биофармацевтическая компания Sarepta Therapeutics сообщила, что зарегистрировала второй случай острой печеночной недостаточности, который привел к…
Продолжить чтение
Регенерация спинного мозга. Первая в мире терапия проходит испытания на людях
Часто пишу о том, что человечество находится в неком переходном состоянии в разрезе развития технологий. То,…
Продолжить чтение
REGENXBIO сообщает о многообещающих результатах испытаний генной терапии
REGENXBIO Inc. (NASDAQ:) поделилась новыми промежуточными данными из текущего клинического исследования фазы I/II AFFINITY DUCHENNE®, оценивающего…
Продолжить чтение
Подросток умер после генной терапии Sarepta Therapeutics
Компания Sarepta Therapeutics сообщила, что подросток с мышечной дистрофией Дюшенна (МДД) умер во время прохождения тщательно…
Продолжить чтение
FDA снимает запрет на проведение КИ терапии болезни Дюшенна компанией Entrada
Компания Entrada Therapeutics продолжит разработку препарата для лечения мышечной дистрофии Дюшенна (МДД) – ENTR-601-44, так как…

Regenxbio подаст заявку на генную терапию дистрофии Дюшенна в 2026 году
RegenxBio объявила о планах подать заявку на получение лицензии на биологические лекарства (biologics licence application, BLA)…
Продолжить чтение
Дувизат: FDA одобрило нестероидное лечение мышечной дистрофии Дюшенна
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило пероральный препарат Дувизат (гивиностат)…
Продолжить чтение
FDA впервые одобрила терапию на основе редактирования генов CRISPR
FDA одобрила два новых препарата для лечения серповидноклеточной анемии у пациентов старше 12 лет. Один из…
Продолжить чтение
Впервые одобрен ваморолон для лечения мышечной дистрофии Дюшенна
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило пероральный препарат Agamree…
Продолжить чтение
FDA одобрило препарат компании Santhera для лечения мышечной дистрофии Дюшенна
Компания Catalyst Pharmaceuticals сообщила, что Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA)…
Продолжить чтение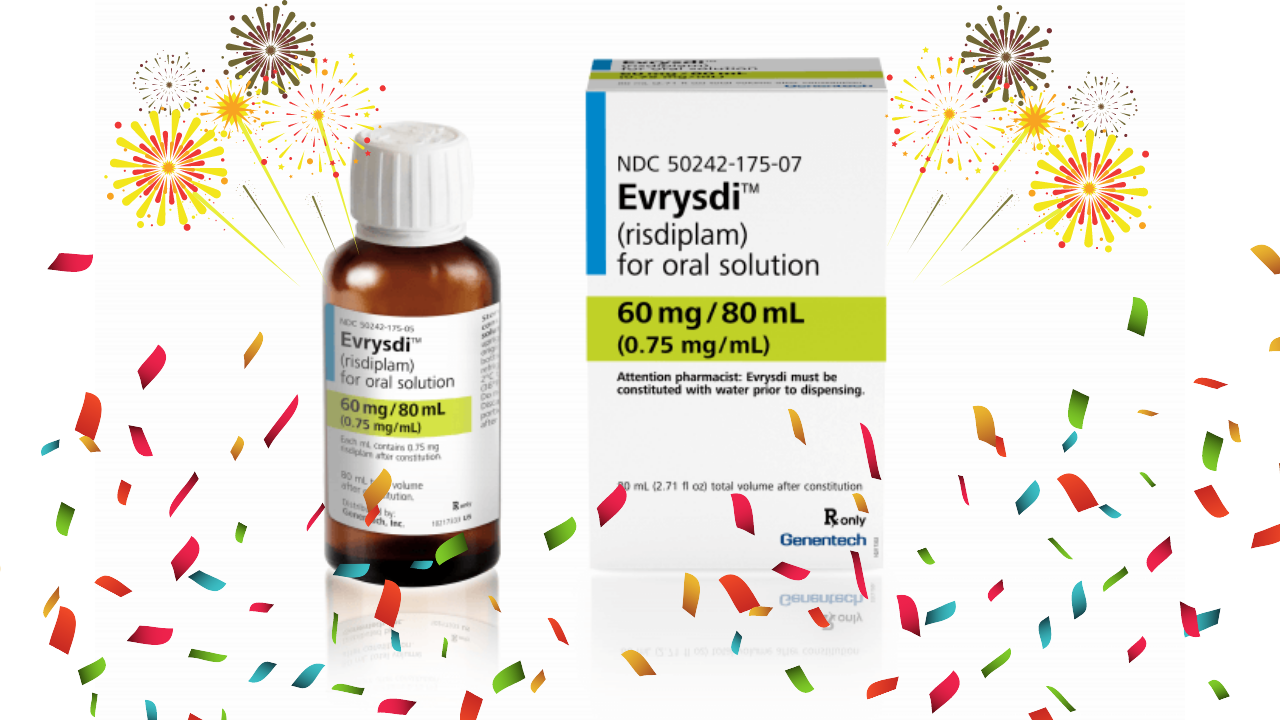
«Эврисди» одобрен в Европе против СМА для новорожденных
Препарат Roche против спинальной мышечной атрофии «Эврисди» одобрили в Европейском Союзе для детей до двух месяцев.…

Генетические ножницы: как из ДНК «вырезают» рак, ВИЧ и другие болезни
CRISPR-Cas9 — эффективный, но не универсальный инструмент генотерапии. Генная терапия возникла в 1990-х годах и за свою короткую историю…
Продолжить чтение
FDA одобрило первый генотерапевтический препарат от миодистрофии Дюшенна за $3,2 млн
Препарат Elevidys от американской Sarepta Therapeutics одобрен FDA по ускоренной процедуре, его клинические исследования еще не…
Продолжить чтение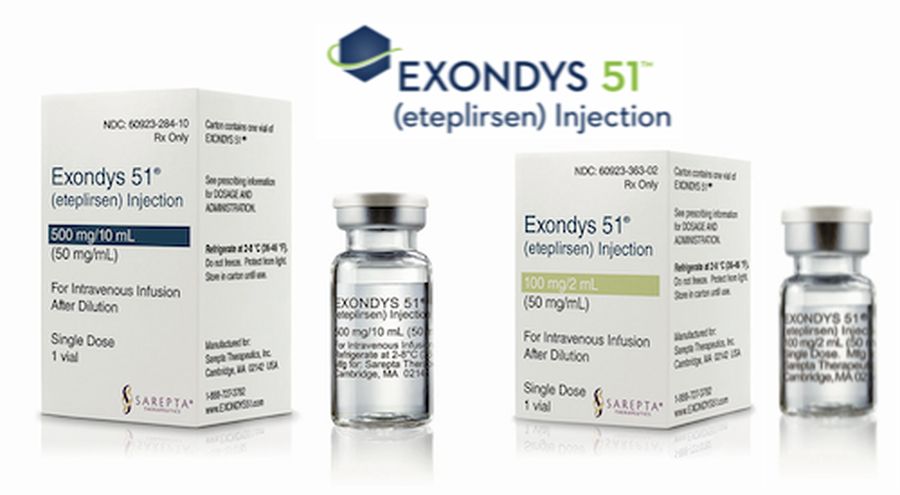
Bloomberg: эффективность 26 лекарств, одобренных FDA по ускоренной схеме, так и не доказана
Агентство Bloomberg выявило 26 препаратов, зарегистрированных Управлением по контролю за продуктами и лекарствами США (FDA) по…
Продолжить чтение
Эксперты FDA сомневаются в эффективности «орфанного» препарата от Sarepta
Эксперты Управления по контролю за продуктами и лекарствами США (FDA) поставили под сомнение эффективность экспериментальной генной…


