FDA рекомендует компании Sarepta возобновить поставки препарата ЭЛЕВИДИС для амбулаторных пациентов с мышечной дистрофией Дюшенна — Компания благодарит…
Продолжить чтениеМетка: Sarepta Therapeutics

Поставки препарата для пациентов с миодистрофией Дюшенна временно приостановят
Компания Roche временно приостановит некоторые поставки в ряд стран за пределы США препарата генозаместительной терапии «Элевидис»,…
Продолжить чтение
Sarepta сообщила о второй смерти пациента после генной терапии
Американская биофармацевтическая компания Sarepta Therapeutics сообщила, что зарегистрировала второй случай острой печеночной недостаточности, который привел к…
Продолжить чтение
Sarepta сообщает о многообещающих результатах исследования ELEVIDYS при лечении мышечной дистрофии Дюшенна
Sarepta Therapeutics, Inc. (NASDAQ:) опубликовала новые данные исследования ENDEAVOR, демонстрирующие обнадеживающие результаты для своего препарата ELEVIDYS,…
Продолжить чтение
Italfarmaco зарегистрирует в ЕС препарат от болезни Дюшенна
Пероральный лекарственный препарат Duvyzat от Italfarmaco получил рекомендацию к одобрению как средство для лечения мышечной дистрофии…
Продолжить чтение
ФАС и «Круг добра» добились снижения цены на первый генный препарат «Элевидис»
Благотворительный госфонд «Круг добра» совместно с Федеральной антимонопольной службой добились значительного снижения цены на первый генотерапевтический…

Подросток умер после генной терапии Sarepta Therapeutics
Компания Sarepta Therapeutics сообщила, что подросток с мышечной дистрофией Дюшенна (МДД) умер во время прохождения тщательно…
Продолжить чтение
Генная терапия мышечной дистрофии Дюшенна от Pfizer провалила финальные клинические исследования
Reuters сообщает о неудачных результатах третьей фазы клинических исследований препарата Ciffreo компании Pfizer. На поздней стадии болезни лечение оказалось не лучше…
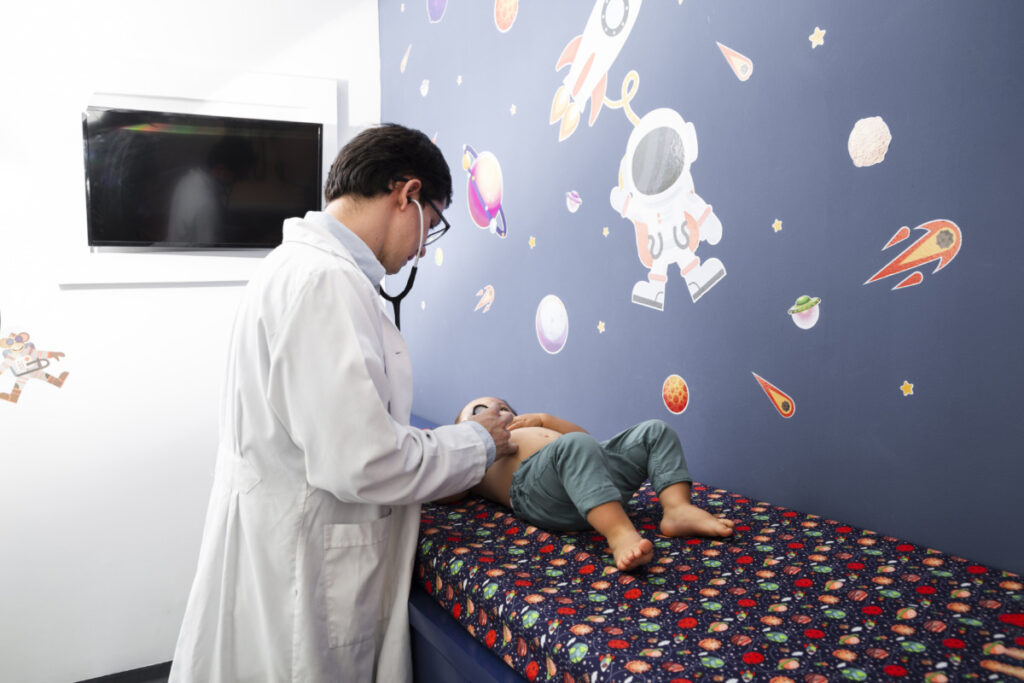
В Петербурге начался пилотный проект по селективному скринингу на мышечные дистрофии Дюшенна и Беккера
Проект позволит обследовать 25 тысяч петербургских мальчиков в возрасте от 12 до 14 месяцев. Это поможет…

FDA одобрило первый генотерапевтический препарат от миодистрофии Дюшенна за $3,2 млн
Препарат Elevidys от американской Sarepta Therapeutics одобрен FDA по ускоренной процедуре, его клинические исследования еще не…
Продолжить чтение
Новый способ лечения редкого генетического заболевания могут одобрить в США
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США собирается одобрить экспериментальный метод лечения…
Bloomberg: эффективность 26 лекарств, одобренных FDA по ускоренной схеме, так и не доказана
Агентство Bloomberg выявило 26 препаратов, зарегистрированных Управлением по контролю за продуктами и лекарствами США (FDA) по…
Продолжить чтение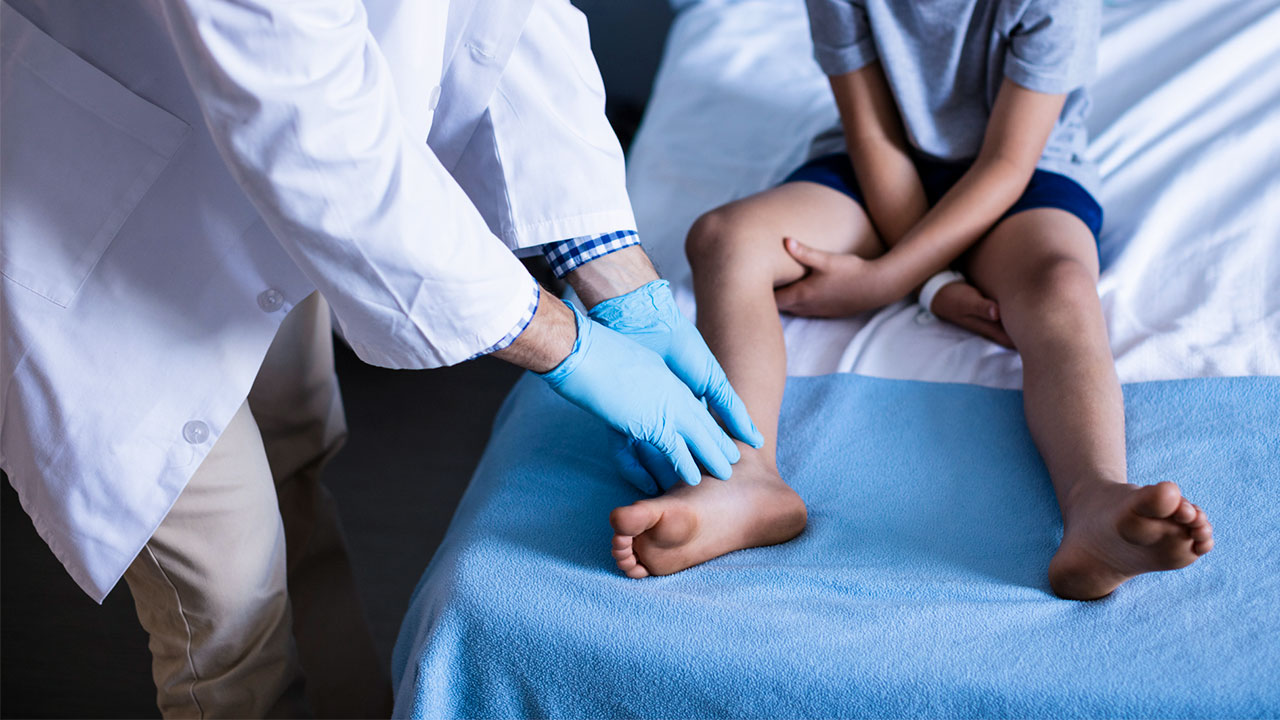
Эксперты FDA сомневаются в эффективности «орфанного» препарата от Sarepta
Эксперты Управления по контролю за продуктами и лекарствами США (FDA) поставили под сомнение эффективность экспериментальной генной…
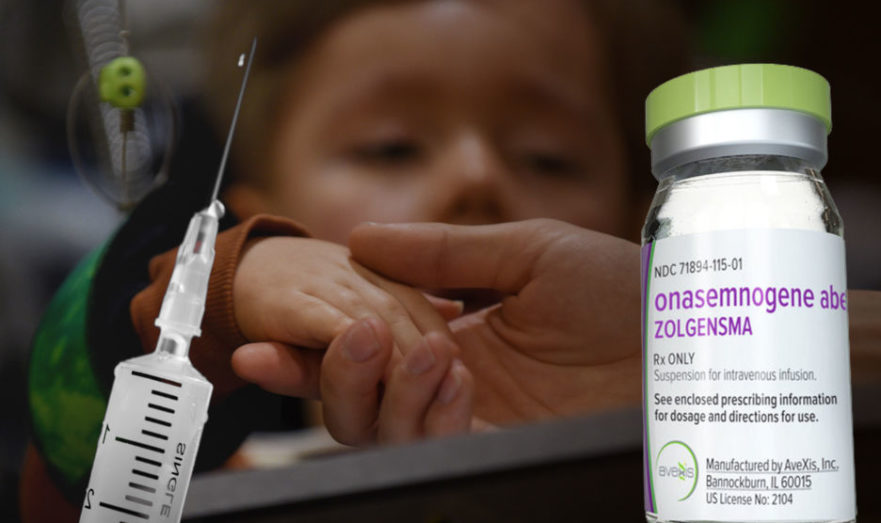
«Круг добра» закупит незарегистрированные препараты для терапии двух редких заболеваний
Экспертный совет фонда «Круг добра» предложил закупить для терапии миодистрофии Дюшенна (МДД) не зарегистрированные в России…
Продолжить чтение
В России начнется исследование нового препарата для лечения болезни Дюшенна
Третий в мире препарат для лечения болезни Дюшенна, разработанный «НС Фарма, Инк.» (NS Pharma, Япония), может…
Продолжить чтение
Голикова рассказала о прототипе технологии лечения миодистрофии Дюшенна
Вице-премьер РФ Татьяна Голикова отчиталась о реализации Федеральной научно-технической программы развития генетических технологий, заявив, что Центр…
Продолжить чтение
Amondys 45: Sarepta утвердила ещё один препарат от мышечной дистрофии Дюшенна
Sarepta Therapeutics объявила о том, что FDA утвердило ее очередной препарат генной терапии. Лекарство, которое будет…
Продолжить чтение
Roche заплатит Sarepta $1,15 млрд за права на препарат генной терапии дистрофии Дюшенна
Швейцарская Roche 23 декабря объявила о заключении лицензионного соглашения с американской биотехнологической компанией Sarepta Therapeutics, касающегося…
Продолжить чтение

