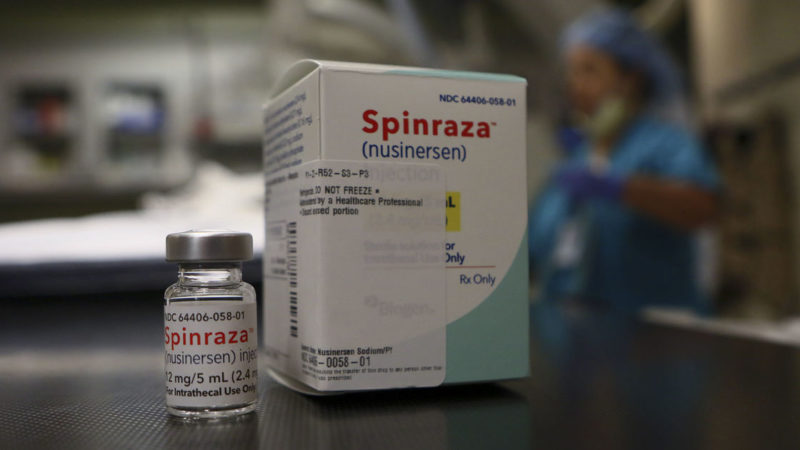
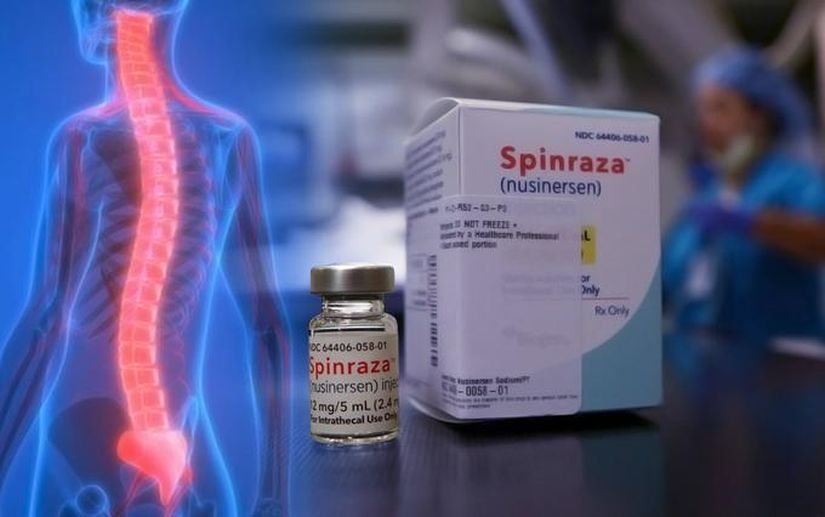
23 декабря 2016 года, FDA объявило , что оно одобрило лекарственный препарат Spinraza™ (nusinersen) для лечения спинальной мышечной атрофии, что делает его первым в истории FDA утвержденных для терапии при SMA.
 Мы очень рады видеть результат усилий нашего сообщества как высшею точку в утверждении Spinraza: не только первый когда-либо одобренный препарат лечения этого заболевания, но и лекарство, которое обращено к основной генетической причине СМА. Это была история всех групп-семей, исследователей, компаний и работы FDA, вместе как одно сообщество, чтобы достичь этой удивительной вехи.
Мы очень рады видеть результат усилий нашего сообщества как высшею точку в утверждении Spinraza: не только первый когда-либо одобренный препарат лечения этого заболевания, но и лекарство, которое обращено к основной генетической причине СМА. Это была история всех групп-семей, исследователей, компаний и работы FDA, вместе как одно сообщество, чтобы достичь этой удивительной вехи.
Нам особенно приятно, что утонченный и строгий план клинический испытаний, который решили реализовать Biogen и Ionis, приведший к масштабному исследованию препарата, позволяющему незамедлительно давать широкий доступ для пациентов.
Одобрение от FDA для всех СМА-детей и взрослых, это широчайшие возможности применения без каких-либо ограничений, и это соответствует ожиданиям нашего сообщества об одном едином лекарства для всех возрастов и всех типов СМА.
«Biogen намерен продолжать работать вместе с сообществом SMA, дальнейших шагов в продолжении исследований применений лекарства, которое уже доказало эффективность лечения этой разрушительной болезни», сказал George A. Scangos, кандидат медицинских наук, главный исполнительный директор компании Biogen. «Команды на Biogen и Ionis благодарны за ту поддержку, которую мы получили, и мы присоединяемся к сообществам Cure SMA и SMA семей в праздновании этой важнейшей вехи.»
«Потребность в лечении спинальной мышечной атрофии возникла давно, так как СМА в настоявшее время является наиболее распространенной генетической причиной смерти у детей раннего возраста, а также болезнью, которая может повлиять на любом этапе жизни,» сказал Billy Dunn, доктор медицинских наук, директор отделения неврологии, продуктов в центре FDA по оценке и исследованиям. «Нашей задачей было проанализировать результаты исследования раньше, чем планировалось. FDA обязуется оказывать помощь в разработке и утверждению безопасных и эффективных препаратов для редких заболеваний, и мы упорно трудились, чтобы рассмотреть это приложение быстро; мы очень рады, что появился первый одобренный препарат для лечения этой изнурительной болезни «.
Главным критерием стали контролируемые клинические исследования, младенцев с СМА получавших SPINRAZA, подтверждающие достижения и поддержание клинически значимых улучшений двигательной функции по сравнению с не получавшими лекарство участников исследования. Кроме того, больший процент выживших больных на SPINRAZA, по сравнению с не получавшими лекарство пациентами.
В открытых исследованиях, некоторые пациенты достигли замечательных результатов, таких как способность сидеть без посторонней помощи, стоять или ходить, эти данные в некоторой степени являются неожиданным. Так как при обычном течении болезни эти способности постепенно утрачиваются с взрослением, приводя к ослаблению и потере этих спосодностей. Общие выводы этих исследований подтверждают эффективность SPINRAZA по всему спектру пациентов SMA. Чем раньше начало лечения, тем заметнее и ощутимее положительный результат, поэтому желательно раннее начало лечения.
Одобрение FDA из SPINRAZA было основано на положительных результатах многочисленных клинических исследований в более чем 170 пациентов. Пакет данных включал промежуточный анализ показателей, трех фаз контролируемого исследования с целью оценки SPINRAZA в младенческом возрасте, а также данные по более взрослым пациентов предварительно симптоматических с или высокой вероятностью развития СМА 1, 2 и 3 типов.
Поздравляем всех СМАшек, родителей и всех причастных к этому волнующему событию. Новый препарат доказал свою эффективность и даёт надежду на лечения спинальной мышечной атрофии. До сих пор СМА было смертельным приговором, теперь у многих появляется шанс выжить. И сделать свою жизнь более комфортной, сгладив неудобства и страдания, которые присуще этому заболеванию.
Адаптивный перевод Виктор Михальченков
Источник http://nnd.name