Исследовательская группа из Университета штата Вашингтон впервые доказала, как работает механизм, заставляющий сердце биться. Этот небольшой процесс на молекулярном уровне может показаться незначительным, но он играет решающую роль в развитии здорового сердца и других мышц.
Нитеподобные белки в клетках сердечной мышцы должны быть точно одинаковой длины, чтобы они могли идеально координироваться, заставляя сердце биться. Другой белок определяет, когда волокно имеет правильный размер, и закрывает цепь маленькой заглушкой. Но если этот белок совершает ошибку и закрывает слишком рано, появляется другой белок, лейомодин, и сбивает ограничение. В молекулярном масштабе процесс выглядит как небольшая игра.
Это открытие может когда-нибудь привести к улучшению диагностики и лечения серьезных и губительных наследственных заболеваний сердца, которые возникают в результате генетических мутаций в белках.
Например, кардиомиопатия, поражает одного из 500 человек во всем мире. Эта группа заболеваний миокарда часто может быть смертельной или иметь длительные последствия для здоровья. Другое подобное заболевание, под названием немалиновая миопатия, поражает скелетную мышечную ткань по всему телу, что часто приводит к тяжелым последствиям.
«Мутации в белках сердечных мышц обнаруживаются у пациентов с миопатией. Наша работа состоит в том, чтобы доказать, что эти мутации вызывают осложнения, и предложить стратегии лечения», — рассказали авторы проекта.
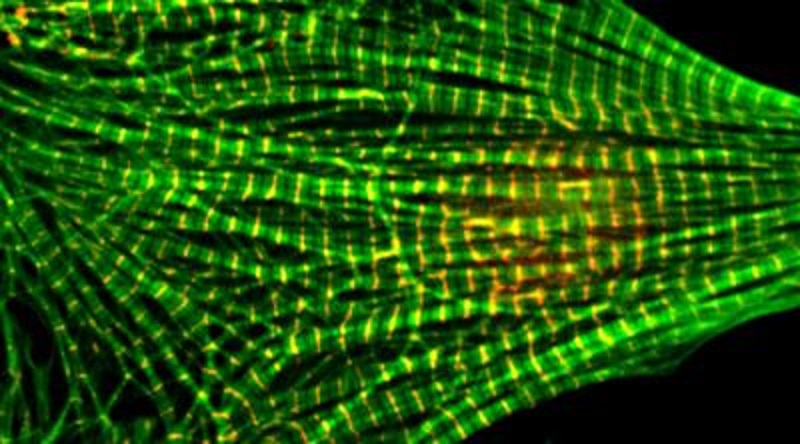
Сердечная мышца состоит из крошечных толстых и тонких нитей белков. С помощью электрических сигналов эти нити завязываются и развязываются, составляя сложную и точную структуру. Этот процесс позволяет сердечной мышце сокращаться и биться.
Тонкие нити состоят из актина, белка, наиболее распространенного в организме человека. Другой белок, тропомизин, обволакивает актиновые филаменты. Тропомиозин вместе с двумя другими белками, тропомодулином и лейомодином, на концах актиновых филаментов действуют как своего рода заглушки и определяют длину образования.
Чтобы сердечная мышца оставалась здоровой, все нити актина, которые имеют длину около микрона, должны быть одинаковой длины. В семьях с кардиомиопатией генетические мутации приводят к образованию слишком коротких или слишком длинных нитей. Пострадавшие могут иметь серьезные проблемы с сердцем, которые приводят к инвалидности, болезни и смерти.
Исследователи изучали этот процесс около семи лет, и доказали, что лейомодин прикрепляется к концу актиновой нити и выталкивает другой белок, тропомодулин, чтобы обеспечить правильную длину актиновой нити. По словам ученых — это первый раз, когда это показано с точностью до атомного уровня
Исследователи надеются продолжить работу и выявить дополнительные компоненты и молекулярные механизмы, которые регулируют структуру тонких волокон.
Статья об исследовании опубликована в журнале Plos Biology.
Источник https://www.computerra.ru




