Недавно журнал Nature Biotechnology отозвал статью 2010 года — о том, как генную терапию для спинальной мышечной атрофии проверяли на лабораторных мышах. С тех пор статью успели 557 раз процитировать и упомянуть по меньшей мере в 59 патентах, а на основании ее выводов — провести клинические испытания и зарегистрировать препарат «Золгенсма». Сейчас в статье нашлись «многочисленные неточности»: данные по выживаемости мышей оказались сомнительными. Выясняем, повлияет ли это на судьбу пациентов, которые уже получили укол «Золгенсмы» или только его ждут.
«Золгенсма» — лекарство-первопроходец. В частности, это один из первых генотерапевтических препаратов против редких наследственных болезней. Большинство одобренных сейчас методов генной терапии лечат заболевания крови, вроде гемофилии. «Золгенсма» нацелена на нервную систему: с помощью аденовирусных частиц она доставляет в двигательные нейроны здоровую копию гена SMN1. И тем самым должна смягчить (а в идеале даже и вылечить) симптомы спинальной мышечной атрофии (СМА) — генетической патологии, при которой группа нейронов спинного мозга постепенно отмирают, а скелетные мышцы, не получая от них сигнала, плохо сокращаются и в итоге атрофируются.
«Золгенсма» не была первым лекарством от СМА, до нее на рынок уже успела выйти «Спинраза». Последний работает по другому принципу: не доставляет новый ген, а корректирует производство белка. Поэтому эффект от нее — временный, и инъекции нужно повторять. «Золгенсма» стала первым лекарством, уколоть которым достаточно всего один раз.
А поскольку одна инъекция должна была решать проблему пациента на всю жизнь, компания «Новартис» (Novartis) назначила своему препарату рекордную по тем временам цену — 2,1 миллиона долларов (о том, почему это не слишком много для лекарства, мы рассказывали в тексте «Укол ценой два миллиона»). Так «Золгенсма» на три года стала самым дорогим лекарством в мире, пальму первенства у нее отобрали только в 2022-м.
За эти три года «Золгенсму» зарегистрировали более чем в сорока странах, а счет пациентов, которые получили «золотой» укол, пошел на тысячи. И только сейчас у ученых возникли сомнения в том, достаточно ли честно этот препарат проверяли изначально.
Вопросы к мышам
Работа 2010 года — типичная проверка нового метода на мышах. Исследователи работали с модельной линией животных, лишенной обеих копий гена SMN. Подопытную группу разделили пополам, каждая половина получила инъекцию аденовирусных частиц: или экспериментальных — с геном SMN, — или контрольных — с геном зеленого флуоресцентного белка.
После этого ученые проверили, что ген действительно добрался до нервных клеток, что он запускает синтез белка, а сами клетки — работают (то есть генерируют импульсы) и устанавливают контакт с мышцами. Дальше за животными наблюдали: как они набирают вес, быстро ли переворачиваются в удобное положение, а главное — сколько живут. И вот на стадии наблюдений что-то пошло не так.
График выживаемости, который исследователи приводят в статье, выглядит очень оптимистично. В то время как 11 контрольных мышей не прожили и месяца, 11 экспериментальных уверенно держались дольше. Одна из них погибла на 97 день по не связанной с болезнью причине, четырех исследователи примерно в это же время усыпили, чтобы оценить состояние нейронов. А оставшимся шести, судя по графику и тексту статьи, к моменту подачи статьи в журнале было уже 250 дней, и умирать они не собирались.
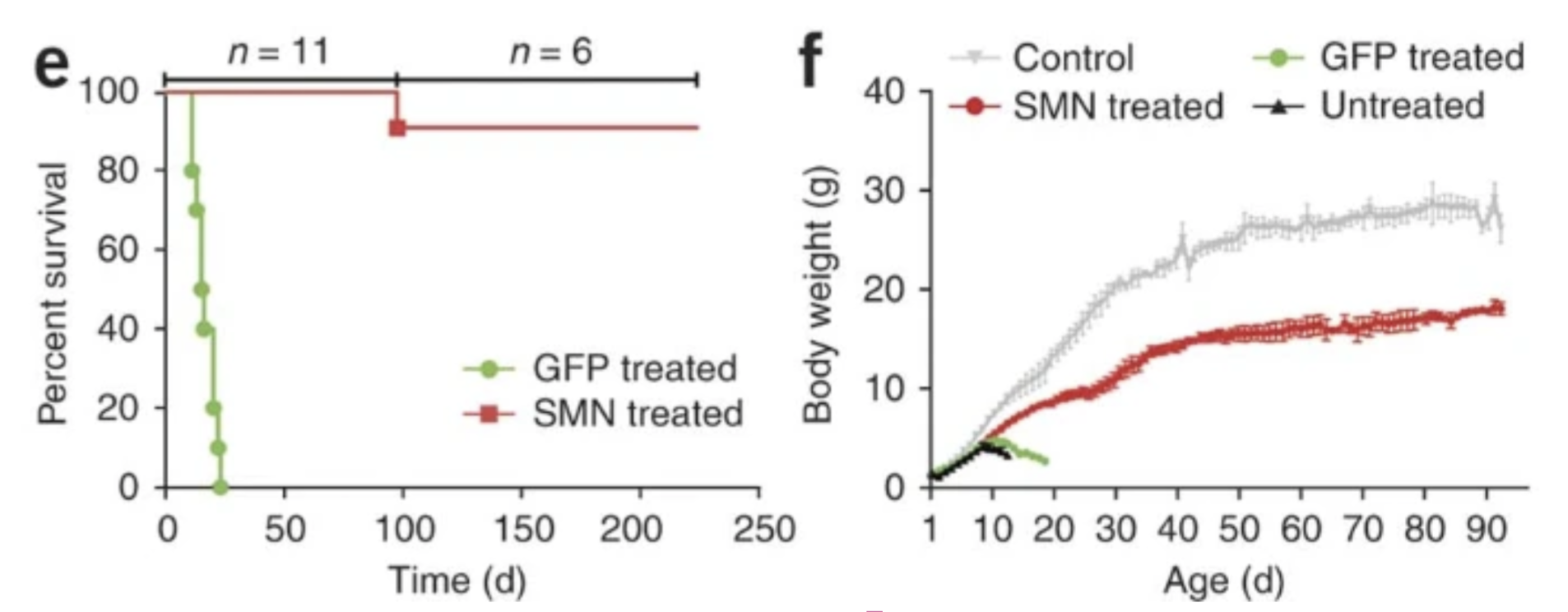
Слева — график с «неточностями». Зеленым обозначена выживаемость контрольной группы, красным — экспериментальной. Справа — масса тела: серым обозначены здоровые мыши, красным — мыши с СМА после лечения, зеленым и черным — мыши с СМА, которые получили ген флуоресцентного белка или вообще никакого лечения
Kevin D Foust et al. / Nature Biotechnology, 2010
Этот график, несмотря на маленькую выборку, означает (хотя и не доказывает окончательно), что терапию можно считать безопасной и эффективной: экспериментальная группа не только живет дольше контроля, но и не погибает от возможных побочных эффектов в долгосрочной перспективе.
Оказалось, что о долгосрочной перспективе судить по этим данным нельзя. 6 октября 2022 года Nature Biotechnology отозвал оригинальную статью и опубликовал пояснительную заметку. Из нее следует, что в 2021 году авторы статьи сами связались с редакцией журнала и сообщили, что обнаружили «неточности» в своих данных о выживаемости мышей. Сами данные на сайте не опубликованы, но из текста заметки следует, что неточности были в том, как авторы измеряли продолжительность жизни мышей и включали животных в выборку. После исправлений выяснилось, что только одна мышь (а вовсе не шесть, как было заявлено) пережила 250 день после лечения.
В результате журнал принял решение снять статью с публикации — потому что «количество неточностей подорвало доверие редакции к этой работе». Авторы работы с этим решением не согласились, но публично его пока никак не прокомментировали. Зато руководство компании «Новартис» заявило, что согласно с отзывом статьи и уже убрало ссылки на нее из своих рекламных материалов.
Ошибки прошлого
«С „Золгенсмой“ это уже второй случай, — говорит руководитель научной экспертизы венчурного фонда LanceBio Venture Илья Ясный. — Это следы предыдущей неаккуратной работы». Три года назад вокруг лекарства уже были споры, очень похожие на то, что происходит сейчас.
24 мая 2019 года FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) одобрило «Золгенсму» для применения — то есть проверило результаты испытаний на мышах и людях и убедилась в том, что препарат безопасен и эффективен. 28 июня в FDA обратились представители «Авексис» (AveXis) — компании, которая придумала и разработала лекарство, после чего ее купил фармгигант «Новартис». Они сообщили, что в данных, которые вошли в заявку для FDA, обнаружили нестыковки. Ошибки нашлись в одном из технических экспериментов, который не был частью доклинических испытаний. Лекарство начали производить по новому протоколу, и нужно было проверить, что оно так же работает на животных, как и первая пробная партия. И вот эту проверку провели небрежно.
FDA отправилось разбираться — и действительно, нестыковки нашлись. Проблема состояла в том, что исследователи неаккуратно записывали результаты наблюдений за мышами, и в отчет попали непроверенные данные. Где-то описанная продолжительность жизни отличалась от реальной на сутки, где-то на двое, а где-то — на целых 19 дней.
Ситуация выглядела подозрительной: компания сообщает о нарушениях всего через месяц после того, как ее продукт одобрили. «Новартис» объяснила это тем, что ее сотрудники обнаружили проблему еще за два месяца до того, как лекарство было одобрено, но после этого проводили свое внутреннее расследование. Расследование держали в секрете, чтобы сами исследователи ни о чем не догадались и не подменили документы, и поэтому оно шло медленно. А закончилось уже после одобрения «Золгенсмы».
В итоге спор решили без ущерба для пациентов. Руководство «Новартис» уволило директора по науке «Авексис», Брайана Каспара, а также заместителя главы компании по научным вопросам Алана Каспара, брата Брайана. И обещало впредь сообщать FDA обо всех новых нарушениях, если они будут обнаружены. А FDA, в свою очередь, приняло решение не отзывать лекарство с рынка: эксперты заключили, что обнаруженные неточности «не влияют на безопасность пациентов или эффективность и качество продукта».
А что же дети
Вопросы к доклиническим исследованиям, которые заставили редакцию Nature Biotechnology отозвать статью, — отголоски той же самой проблемы. Речь, конечно, идет о разных экспериментах: в одном случае проверяли, работает ли препарат в принципе, а во втором — не перестал ли он работать после изменений в процессе производства. Но «неточности» абсолютно те же: снова неаккуратные данные, неучтенные мыши, и главный автор статьи — тот же Брайан Каспар.
Такая история — скорее редкость для крупных фармкомпаний. «Я [других] таких прецедентов не припомню, — говорит Ясный. — Обычно если фальсификации обнаруживаются, то это манипуляции с данными клинических исследований, и тогда лекарство не пускают на рынок. А тут нарушения небольшие и не влияющие на профиль пользы и риска, но неприятные для репутации».
Тем не менее, для практикующих врачей и репутация лекарства, кажется, не изменилась. «Меня как для клинициста и врача, который имеет свою практику, эта статья не сильно настораживает», — говорит Светлана Артемьева, заведующая отделением психоневрологии в НИКИ педиатрии и детской хирургии имени Вельтищева. По ее словам, данных клинических испытаний на людях вполне достаточно, чтобы оценить и безопасность, и эффективность, независимо от результатов на мышах.
При этом данных о выживаемости пациентов с СМА после лечения «Золгенсмой» пока довольно мало. Поскольку лекарство молодое, даже за самыми первыми участниками испытаний, которые его получили, врачи наблюдают около 6,5 лет. И судить о том, как лечение повлияет на их жизнь в подростковом и взрослом возрасте, пока рано. К тому же, на первых этапах испытаний, как это часто бывает, выборка была маленькая — всего 15 человек.
Артемьева рассказывает, что, в отличие от мышей, добиться стопроцентной выживаемости детей, которых лечат «Золгенсмой», не удается. Лекарство начинает действовать не сразу, поэтому прогноз зависит от того, насколько грамотно врачи ведут ребенка уже после укола «Золгенсмой». «Когда мы начинаем лечить тяжелого ребенка со СМА I типа, — говорит она, — мы рекомендуем все равно продолжать респираторную поддержку, следить за кормлением, чтобы не было аспирации, потому что нужно время на восстановление нервной системы».
В некоторых случаях, по ее словам, не удается правильно оказать дыхательную поддержку — но относить это к побочным эффектам препарата не стоит. Поэтому Артемьева полагает, что отзыв статьи на мышах не подорвет доверие к препарату, и его продолжат назначать пациентам.
Илья Ясный тоже считает, что неточности в статье — пусть даже той, что послужила фундаментом для клинических испытаний, — не повлияют на судьбу «Золгенсмы». «Здание устоит, — уверен он, — потому что пролечено уже более 2300 детей, и клинические данные имеют приоритет над доклиническими. Траектория развития леченых детей намного опережает исторический контроль: они начинают ходить, говорить, чего от нелеченых ожидать было нельзя».
FDA пока никак не реагировало на отзыв статьи, но представители «Новартис» не опасаются ущерба для компании. А если последствий для «Золгенсмы» действительно не будет, то можно будет констатировать: это только кажется, что современная фармакология стоит на плечах мышей. Как только очередное здание достроено и лекарство появляется на прилавках, мышей из фундамента можно смело убирать — без ущерба для всей остальной конструкции.
Источник nplus1.ru