Биологи из университета Беркли и Национальной Лаборатории Лоуренса вместе с коллегами из Токийского университета разработали новый способ доставки в клетки CRISPR-систем, редактирующих геном. Белок Cas9 вместе с направляющей РНК (gRNA) и донорской ДНК (dDNA) прикрепляли к золотым наночастицам и окружали специальным заряженным полимером, получая комплекс, эффективно проникающий в клетки и доставляющий одновременно все необходимые макромолекулы к заданной цели. В результате такой инструмент оказался способен редактировать мутации, например, в гене, мутации в котором вызывают мышечную дистрофию Дюшенна, не выключая его, а осуществляя репарацию за счет гомологичной рекомбинации и добиваясь восстановления правильной последовательности гена. Исследование опубликовано в Nature Biomedical Engineering.
Геномное редактирование может стать решением при борьбе с множеством заболеваний, в том числе хронических. Система редактирования генома CRISPR-Cas9 (подробно о ней можно почитать в нашем материале), впервые разработанная для применения в лаборатории одним из соавторов данной работы, Дженнифер Дудной и ее коллегами, предлагает на данный момент две основных методики: вырезание куска гена, ведущее к его выключению; или гомологичная рекомбинация, в результате которой последовательность гена с мутацией заменяется на правильную, и ген начинает работать так, как работает у здорового человека. Вторая методика, несмотря на очевидные свои преимущества, пока что применяется редко, поскольку в лабораторных условиях редко удается достичь нужного уровня ее эффективности и безопасности. Это связано, в частности, с тем, что она требует доставки к мутированной ДНК одновременно нескольких макромолекул: белка Cas9, который будет узнавать последовательность с мутацией и резать ее, gRNA (направляющей РНК, в которой записана мутация для узнавания) и dDNA (донорская ДНК). На данный момент в экспериментах с мышечной дистрофией Дюшенна у мышей, где система CRISPR-Cas9 вводилась в организм животных напрямую, удавалось достичь лишь 0,3 процентов эффективности редактирования гена дистрофина, мутации в котором вызывают данное неизлечимое смертельное заболевание.
Одним из альтернативных методов доставки системы CRISPR-Cas9 в организм является упаковка ее в аденовирусные частицы, однако здесь возникают новые трудности: у большинства людей, например, в ответ на попадание таких вирусных частиц в организм начинается сильная иммунная реакция; кроме того, используемые частицы часто недостаточно велики и материал приходится распределять в них неравномерно, что снижает эффективность его доставки.
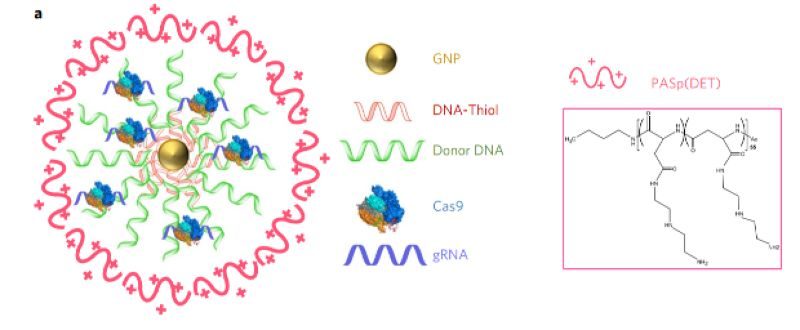
В данной работе ученые использовали золотые наночастицы, к которыми связывали тиол-ДНК, а затем гибридизовали ее с dDNA. Затем к этой системе крепились за счет аффинности к ДНК комплексы Cas9 с gRNA (RNP); наконец, снаружи наносился положительно заряженный полимер (poly(N-(N-(2-aminoethyl)-2-aminoethyl) aspartamide) PAsp(DET), обеспечивающий электростатические взаимодействия внутри комплекса, повышающие его стабильность.
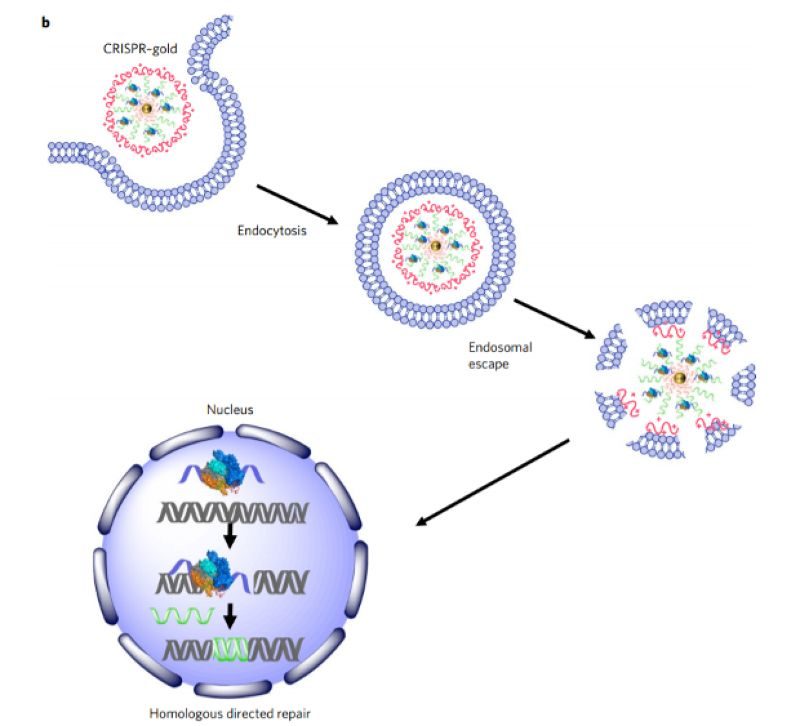
Комплекс, как было показано отдельно, проникал в клетки за счет кавеолярного эндоцитоза, после чего PAsp(DET) разрушал эндосомы, и все компоненты CRISPR-Cas9 системы оказывалась внутри клетки одновременно. Серия экспериментов in vitro с клетками человека и мыши показала, что система успешно проникает в клетки и редактирует заданные гены.
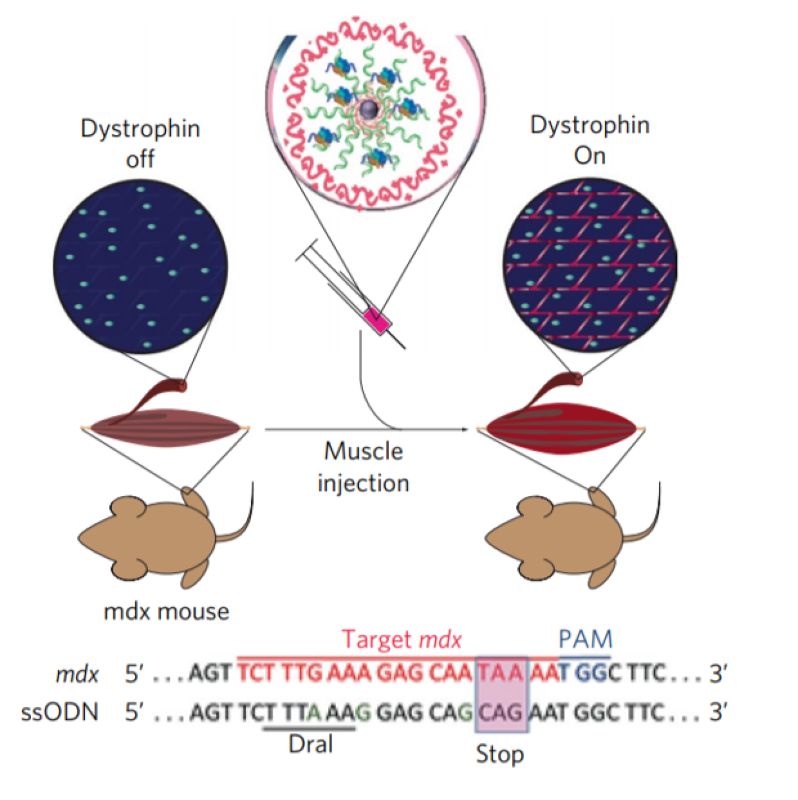
После этого ученые провели исследование с живыми мышами, больными мышечной дистрофией Дюшенна и анализируя воздействие CRISPR-Cas9 на ген дистрофин после одной инъекции. Выяснилось, что эффективность редактирования гена золотыми наночастицами в 18 раз выше, чем при непосредственном введении системы в организм (5,4 процентов успешно отредактированных генов против 0,3 процентов). Более того, стандартный тест для мышей, определяющий их способность висеть на четырех конечностях в течение определенного времени продемонстрировал в два раза лучшие показатели по сравнению с этим контролем. Уровень фиброза в мышечных тканях мышей также заметно снизился. Ученые отмечают, что это свидетельствует о существенном прогрессе в лечении заболевания.
Дополнительные исследования показали, что введение золотых наночастиц не приводит к значительным вспышкам иммунного ответа, как это бывает при введении вирусных носителей, хотя уровень лейкоцитов CD45+ и CD11+ в организме несколько повышается. Кроме того, ученые выяснили, что даже многократное введение золотых наночастиц не вызывает усиления синтеза противовоспалительных цитокинов и потери веса.
Доставка CRISPR-Cas9 систем в вирусных частицах также бывает связана с последующим излишне высоким уровнем синтеза Cas9 в клетках, что может приводить к неправильному ходу его работы и изменению хозяйской ДНК в произвольных местах (подробнее о таких неучтенных мутациях можно прочитать здесь). Доставка системы в золотых наночастицах, однако, не предполагает дополнительного синтеза Cas9, и оценка количества случайных мутаций после проведения таких инъекций показала, что уровень мутаций не превышает обычные показатели нормы (0,005 — 0,2 процента).
В будущем ученые собираются проводить клинические исследования, конечной целью которых будет являться разработка лекарственных препаратов для лечения человеческих болезней (в США разрешили редактирование человеческого генома еще в 2016 году, и первые эксперименты с эмбрионами уже опубликованы, хотя пока что такие эмбрионы еще нельзя вынашивать). Для этого, в частности, соавторами статьи был открыт стартап GenEdit. А лаборатория в Беркли сейчас занимается разработкой новых наночастиц, которые будут доставлять системы для редактирования генома непосредственно в стволовые клетки.